Portale "Ingegneria e Campanologia" - Autore - Sommario - Mappa del Sito - Home
Proprietà e metallurgia del Rame
AREA I - ARTE TECNICO-SCIENTIFICA (ATS)
Cap. ATS-G06 - Proprietà metalli - Pag. ATS-G06.01
Gli argomenti trattati sono stati inseriti da Ing. Arch. Michele Cuzzoni nel 2012 - © Copyright 2007- 2025- e sono desunti dalla documentazione indicata in Bibliografia a fondo pagina
E’ un metallo che si ricava dalla calcopirite, dalla calcosina o dalla cuprite. Oppure si trova allo stato puro sottoforma di rame nativo. La produzione con Cu al 99% avviene attraverso la fusione del minerale con l’aggiunta di reagenti chimici in modo successivo, finché il rame diventa molto affinato (99,7%- 99,9%). Il resto è costituito da ossigeno; resiste alla corrosione e rimane inalterato nel tempo. Può essere anche riutilizzato.
I principali stati di ossidazione sono +1 e +2. I potenziali standard sono positivi per tutte le coppie seguenti:
![]()
Il rame metallico è ossidato solo da energici ossidanti, come l'acido nitrico, e anche dall'acido solforico concentrato a caldo:
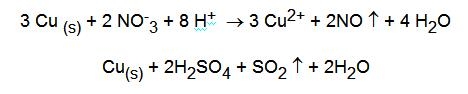
I sali rameosi sono generalmente instabili. In soluzione il rame (I) è in grado di esistere solo a basse concentrazioni, altrimenti dismuta a rame(0) o rame (II):
![]()
Per questo motivo esso è stabile solo in composti poco solubili o in complessi stabili, in molecole cioè che realizzano una bassa concentrazione di Cu + in soluzione.
I sali rameosi sono quasi tutti insolubili: CuCN, CuCl, CuI (tutti bianchi) CuBr, giallo chiaro e Cu2S nero.
A pH = 3 precipita l'idrossido CuOH, giallo, che si trasforma rapidamente in Cu2O, giallo:
![]()
Forma molti complessi, soprattutto con ammoniaca, cianuri e cloruri.
Il catione rameico esiste libero in soluzione a pH < 5. E' di color azzurro tenue e precipita come Cu(OH)2 che si ridiscioglie solo a pH molto elevati con formazione di anioni di color blu del tipo [Cu(OH)4]2- o con strutture più complesse. I sali sono quasi tutti molto solubili. Tra i più insolubili si ricordano CuS, un altro solfossido, nero, e il complesso Cu2[Fe(CN)6], rosso scuro. Da ricordare anche il tetraamminorame(II), [Cu(NH3)4]2+, di color blu intenso.
Le più importanti reazioni analitiche si hanno:
- con H2S : precipita CuS, nero, solubile in acido nitrico 6 N;
- con ammoniaca: si ottiene una soluzione intensamente colorata in blu per la formazione di [Cu(NH3)4]2+;
- con K4[Fe(CN)6]: precipita Cu2[Fe(CN)6], rosso scuro.
Data la sua alta conducibilità elettrica il rame metallico trova un vastissimo uso come conduttore elettrico.
Importanti sue leghe sono i
![]() bronzi e gli
bronzi e gli
![]() ottoni. La
Lega di Devarda, costituita dal 50% di rame, dal 45% di alluminio e dal 5% di
zinco è facilmente polverizzabile e si usa nell'analisi qualitativa per la
ricerca dei nitriti e dei nitrati, i quali vengono da essa ridotti ad ammoniaca
in soluzione alcalina.
ottoni. La
Lega di Devarda, costituita dal 50% di rame, dal 45% di alluminio e dal 5% di
zinco è facilmente polverizzabile e si usa nell'analisi qualitativa per la
ricerca dei nitriti e dei nitrati, i quali vengono da essa ridotti ad ammoniaca
in soluzione alcalina.
L’umidità dell’aria forma una patina superficiale, chiamata di "bronzo antico", di idrocarbonato di rame.
Se il rame viene riscaldato al contatto dell’aria, prima si ricopre di uno strato rosso, poi nero.
Molto plastico il rame si incrudisce rapidamente alla martellatura, divenendo fragile (incrudimento), per cui deve essere ricotto, cioè riscaldato al fine di ottenere la ricristallizzazione e la riduzione delle tensioni interne al materiale, annullando gli effetti dell’incrudimento.
Ha una buone malleabilità e duttilità può essere ben lavorato a freddo e ha un’ottima conducibilità elettrica. Molto utilizzato in elettronica ed elettrotecnica.
|
Simbolo chimico |
Cu |
|
Temperatura di fusione |
1083°C |
|
Massa volumica |
8900 Kg/m3 |
Metallo rossastro della densità di 8,8 (8,790 alla fusione) e con un punto di fusione verso i 1100°. Punto di ebollizione 2100°.
Tuttavia piccole quantità di impurità esercitano una grandissima influenza sulla sua composizione finale e sulle sue proprietà.
Colato troppo caldo produce delle soffiature.
Per colarlo in lingotti e per evitare le soffiature si aggiunge, prima di colarlo, il 2% di magnesio metallico. Il magnesio (densità 1,75; punto di fusione 759°-800°) di tutti i metalli è quello che ha più affinità con l’ossigeno. E’ quindi il miglior riducente o diossidante nella fusione delle diverse leghe contenenti rame, nichel, stagno, alluminio, zinco, piombo, ecc.
Per uso fonderia con il rame conviene il magnesio in forma di bacchette. Questo agisce non solo quale riducente dell’ossidulo di rame, ma forma altresì dei composti con le impurità contenute nel rame stesso, che restano così eliminate sotto forma di scorie con miglioramento delle qualità meccaniche del metallo (resistenza, allungamento).
Già in antico si comprese che per migliorare le qualità del rame bisognava aggiungere degli elementi quali l’arsenico e il fosforo che non potevano essere isolati nell’antichità, è probabile quindi che si adoperassero minerali arsenicati (solfuro o arseniuro) o fosforosi.
|
DESIGNAZIONE RAME |
|||||||||
|
Designazione UNI 5649 |
Composizione chimica |
Tipo di rame |
|||||||
|
Cu+Ag |
Cu+Ag+As |
Bi |
Pb |
P |
|
||||
|
Cu-CATH |
99,90 |
- |
0,001 |
0,005 |
- |
As 0,0015 |
Rame elettroilitico e sotto forma di catodi |
||
|
Cu-OF |
99,95 |
- |
- |
- |
- |
- |
Colato nelle forme commerciali adatte alle successive lavorazioni
|
Ottenuto da Cu-CATH esente da ossidalo di rame |
|
|
Cu-ETP |
99,90 |
- |
0,001 |
0,005 |
- |
O2 0,04 |
Ottenuto da Cu-CATH Obtained out of Cu-CATH |
||
|
Cu-DLP |
99,90 |
- |
0,001 |
0,01 |
0,004 0,012 |
- |
Basso residuo di P |
Disossidato, ottenuto da rame elettrolitico o termico |
|
|
Cu-DHP |
99,90 |
- |
0,001 |
0,01 |
0,013 0,050 |
- |
Alto residuo di P |
||
|
Cu-LSTP |
99,90 |
- |
0,001 |
0,005 |
- |
Ag 0,02 0,12 |
Basso Contenuto di Ag |
Ottenuto da Cu-CATH con aggiunta di Ag |
|
|
Cu-HSTP |
99,90 |
- |
0,001 |
0,005 |
- |
Ag 0,12 0,25 |
Alto Contenuto di Ag |
Ottenuto per raffinazione termica |
|
|
Cu-FRTP |
99,80 |
- |
0,002 |
0,01 |
0,05 |
- |
Ottenuto per raffinazione termica |
||
|
Cu-DPA |
99,40 |
99,70 |
0,002 |
0,01 |
0,013 0,050 |
As 0,15 0,50 |
Ottenuto da rame elettrolitico con aggiunta di Ag |
||
|
UNI 5649 |
APPLICAZIONI |
|
|
Cu-CATH |
Per semilavorati |
Deve essere fuso in forma colata per le successive lavorazioni. Utilizzato nella produzione di conduttori elettrici e leghe pregiate. |
|
Cu-OF |
Per l’industria elettronica e per esigenze di massima lavorabilità plastica a freddo. Per conduttori elettrici e leghe pregiate. |
|
|
Cu-ETP |
||
|
Cu-DLP |
Per semilavorati per i quali non vi sono esigenze di conduttività elettrica ma aventi buona lavorabilità plastica ed esenti da fenomeni di fragilità in ambiente riducente. |
|
|
Cu-DHP |
||
|
Cu-LSTP |
Per semilavorati o getti |
Per conduttori ove l’Ag eleva la temperatura di cristallizzazione (ricottura) del rame. |
|
Cu-HSTP |
||
|
Cu-FRTP |
Senza esigenze di conduttività elettrica, buona deformabilità e saldabilità, non fragile in ambiente riducente se ossidato al fosforo. |
|
|
Cu-DPA |
Elevate temperature in ambiente ossidante. Piastre per focolari e in genere per parti di impianti termici, bruciatori, ecc. |
|
|
DENOMINAZIONE E SIGLE |
|||||
|
ISO |
UNI |
BS |
AFNOR |
DIN |
ASTM |
|
Cu-CATH |
Cu-CATH 5649/3-88 |
Cu-CATH-2 |
|
KE-Cu 2.0050 1708 |
CATH B 115-83 |
|
Cu-ETP |
Cu-ETP 5649/1-88 |
Cu-ETP C 101 6017 :1981 |
Cu-a1 51-50 1983 |
E-Cu 57 2.0060 1787 E-Cu 58 2.0065 1787 |
ETP C 11000 |
|
Cu-FRHC |
Cu-FRHC 5649/1-88 |
Cu-FRHC C 102 6017 :1981 |
Cu-a2 51-50 1983 |
|
FRHC C 11020 |
|
Cu-OFE |
|
Cu-OFE C 110 6017 :1981 |
Cu-c2 51-50 1983 |
|
OFE C 10100 B 170-82 |
|
Cu-OF 1337 – 1980 (E) |
Cu-OF 5649/1-88 |
Cu-OF C 103 6017 :1981 |
Cu-c1 51-50 1983 |
OF-Cu 2.0040 1787 |
OF C 10200 B 170-82 |
|
Cu-HCP 431 – 1981 |
Cu-HCP 5649/1-88 |
|
|
SE-Cu 2.0070 1787 |
OFXLP C 10300 B 379-80 |
|
Cu-DLP 1337 – 1980 (E) |
Cu-DLP 5649/1-88 |
|
Cu-b2 51-50 1983 |
SW-Cu 2.0076 1787 |
DLP C 12000 |
|
Cu-DHP 1337 – 1980 (E) |
Cu-DHP 5649/1-88 |
Cu-DHP C 106 6017 :1981 |
Cu-b1 51-50 1983 |
SF-Cu 2.0090 1787 |
DHP C 12200 B 379-80 |
|
|
Cu-Ag 0,055649/2-88 |
|
Cu-Ag 0,05 |
|
|
|
|
Cu-Ag 0,1 5649/2-88 |
|
Cu-Ag 0,1 |
Cu Ag 0,1 2.1203 17666 |
|
|
Cu-Ag 0,05 (OF) 1336 – 1980 (E) |
Cu-Ag 0,05 (OF) 5649/2-88 |
|
Cu-Ag 0,05 (OF) |
|
|
|
Cu-Ag 0,1 (OF) 1336 – 1980 (E) |
Cu-Ag 0,1 (OF) 5649/2-88 |
|
Cu-Ag 0,1 (OF) |
|
|
|
Cu-Ag 0,05 (P) 1336 – 1980 (E) |
Cu-Ag 0,05 (P) 5649/2-88 |
|
Cu-Ag 0,05 (P) |
|
|
|
Cu-Ag 0,1 (P) 1336 – 1980 (E) |
Cu-Ag 0,1 (P) 5649/2-88 |
|
Cu-Ag 0,1 (P) |
Cu Ag 0,1 P 2.1191 17666 |
|
|
|
Cu Cd 0,5 5649/2-88 |
C 108 |
|
|
C 16200 |
|
|
Cu Cd 1 5649/2-88 |
|
|
|
|
|
|
Cu As (P) 5649/2-88 |
C 107 |
|
|
DPA C 14200 B 379-80 |
|
|
Cu S (P 0,01) 5649/2-88 |
C 111 |
Cu-S (P 0,01) |
Cu S P 2.1498 17666 |
|
|
|
Cu S (P 0,03) 5649/2-88 |
|
Cu-S (P 0,03) |
|
C 14710 |
|
|
Cu Te (OF) 5649/2-88 |
|
|
|
|
|
|
Cu Te (P) 5649/2-88 |
C 109 |
Cu-Te (P) |
Cu Te P 2.1546 17666 |
DPTE C 14500 |
|
CARATTERISTICHE ELETTRICHE DEL RAME |
||||
|
RAME UNI 5649-1 |
RESISTIVITÀ DI MASSA W x g/m2 max. |
RESISTIVITÀ DI VOLUME W x g/m2 max. |
CONDUTTIVITÀ |
|
|
m/Ohm x mm2 |
IACS % min |
|||
|
Cu-ETP |
0,15328 |
0,017241 |
58,00 |
100 |
|
Cu-FRHC |
0.15328 |
0,01241 |
58,00 |
100 |
|
Cu-OF |
0,15328 |
0,017241 |
58,00 |
100 |
|
Cu-HCP |
0,15614 |
0,017565 |
56,93 |
98,16 |
|
Cu-DLP |
0,158 » |
0,0178 » |
56 » |
97 » |
|
Cu-DHP |
0,222 » |
0,025 » |
40 » |
69 » |
|
N.B. I valori riportati sono riferiti allo stato fisico ricotto. |
||||
|
CARATTERISTICHE MECCANICHE DEL RAME |
||||||
|
Stato fisico |
Sezione (barre poligonali) mm2 |
Dimensione (barre tonde) mm |
Carico di rottura N/mm2 |
Carico di snervamento N/mm2 |
Allungamento % min |
Durezza Brinell HB |
|
Estruso grezzo |
Tutte |
Tutte |
> 195 |
|
30 |
< 50 |
|
Trafilato ricotto |
Tutte |
Tutte |
195÷245 |
|
40 |
40÷60 |
|
Trafilato semicrudo |
< 1200 |
< 50 |
245÷295 |
|
12 |
70÷90 |
|
> 1200 |
> 50 |
> 230 |
|
15 |
> 65 |
|
|
Trafilato crudo |
< 200 |
< 14 |
295÷365 |
> 255 |
7 |
90÷110 |
|
200 < s < 600 ----------------- 600 < s < 1200 |
14 < d < 24 24 < d < 60 60 < d < 95 |
> 295 > 285 > 275 |
> 255 > 215 > 205 |
10 12 12 |
85÷100 80÷95 70÷90 |
|
|
> 1200 |
> 95 |
> 225 |
> 165 |
15 |
70÷90 |
|
Portale "Ingegneria e
Campanologia" -
Autore -
Sommario
- Mappa del Sito -
Home
Bib-TS-010 - M. Cavallini, F. Iacoviello - Materiali Metallici - Francesco Ciolfi Editore, via E. De Nicola, Cassino
Bib-TS-011 - W. Nicodemi - Metallurgia - Masson, Milano
Bib-TS-012 - A. Cigada - Struttura e proprietà dei materiali metallici - Città Studi, Milano
Bib-TS-092 - L. Mugnani - Manuale pratico di fonderia - Milano, 1928
Bib-TS-093 - Dispense di Chimica - A.A. 1992/1993 - Facoltà di Ingegneria Edile / Architettura - Pavia