Portale "Ingegneria e Campanologia" - Autore - Sommario - Mappa del Sito - Home
Proprietà e metallurgia del Ferro
AREA I - ARTE TECNICO-SCIENTIFICA (ATS)
Cap. ATS-G03 - Proprietà metalli - Pag. ATS-G03.03
Gli argomenti trattati sono stati inseriti da Ing. Arch. Michele Cuzzoni nel 2008 - © Copyright 2007- 2025- e sono desunti dalla documentazione indicata in Bibliografia a fondo pagina
I metalli sono caratterizzati da una particolare struttura cristallina per cui gli elettroni non sono rigidamente associati ai nuclei nei rispettivi atomi, ma sono liberi di muoversi.
Questa caratteristica determina elevata conducibilità elettrica e termica.
A temperatura ambiente si presentano allo stato solido; hanno elevato peso specifico, sono malleabili, duttili e opachi. I metalli puri vengono usati poco, sono più usate le leghe.
Il ferro puro è di colore bianco-argenteo, è duttile e malleabile.
Il carbonio ha peso atomico 12,01 ed esiste in natura in tre forme caratterizzate da diversa struttura cristallina: il diamante,la grafite e il carbonio amorfo.
Queste forme:
-
hanno punti di fusione estremamente alti.
-
i più comuni fra i suoi composti sono quelli che contengono carbonio e idrogeno (idrocarburi).
Il carbonio è poco reattivo a temperatura ambiente, ma a temperature elevate reagisce facilmente con molti metalli per formare i carburi, e con l'ossigeno per formare il monossido di carbonio (CO) e il diossidodi carbonio, noto anche come anidride carbonica (CO2).
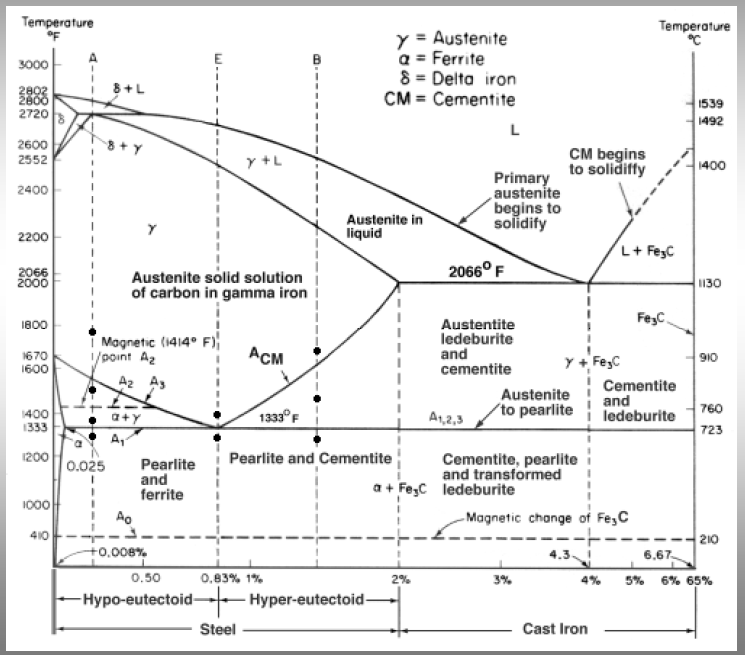
Consideriamo diversi raffreddamenti della lega Fe-C a diverse concentrazioni di Carbonio.
La verticale per A corrisponde ad una percentuale di C pari circa a 0,4%.
La lega comincia a solidificare (1500°C), si cominciano a formare i primi grani di austenite, ovvero ferro gamma in cui è presente una soluzione di carbonio.
Continuando a raffreddare, secondo e terzo punto in grassetto, si libera dall’austenite la ferrite, ferro in forma alfa.
Al di sotto della temperatura di 723°C l’austenite si trasforma in perlite ovvero ferrite con lamelle di cementite, questo perché la cementite è solubile nel ferro gamma ma non nel ferro alfa.
L’eutettoide è il punto cui corrisponde una lega composta da carbonio allo 0,8% in cui avviene la completa trasformazione del ferro dalla forma alfa a quella gamma.
La verticale per B corrisponde ad 1,4% circa di carbonio.
La solidificazione dell’austenite finisce al primo punto in grassetto, continuando a raffreddare si libera cementite disciolta in ferro gamma e raffreddando ancora l’austenite si trasforma in perlite.
Ad una percentuale di carbonio del 3% l’austenite solidifica mantenendo una percentuale di carbonio del 2,08% ed il resto della fase liquida solidifica in ledeburite, un composto formato da cementite all’interno dell’austenite. Questo fino alla temperatura di 723°C al di sotto della quale si libera cementite.
Se la lega presenta lo 0,8% di carbonio tutta l’austenite si trasforma in perlite a 723°C.
Se la lega presenta 4,3% di carbonio tutta l’austenite solidifica in ledeburite.
Le leghe che presentano una % di carbonio superiore al 4,3% non interessano poiché hanno scarse proprietà meccaniche
Portale "Ingegneria e
Campanologia" -
Autore -
Sommario
- Mappa del Sito -
Home
Bib-TS-092 - L. Mugnani - Manuale pratico di fonderia - Milano, 1928
Bib-TS-094 - ICCROM - Ancient metals – Metaux anciens - Roma, 1980
Bib-TS-095 - C. Giardino - I metalli nel mondo antico - Bari, 1998