Portale "Ingegneria e Campanologia" - Autore - Sommario - Mappa del Sito - Home
Analisi chimiche per materiali e metalli
AREA I - ARTE TECNICO-SCIENTIFICA (ATS)
Cap. ATS-F03 - Chimica - Pag. ATS-F03.11
Gli argomenti trattati sono stati inseriti da Ing. Arch. Michele Cuzzoni nel 2012 - © Copyright 2007- 2025- e sono desunti dalla documentazione indicata in Bibliografia a fondo pagina
- Generalità
- Spettroscopia di assorbimento atomico
- Spettroscopia di emissione atomica
- Spettroscopia di fluorescenza di raggi x
- Fluorescenza di raggi X
- Diffrazione di raggi X
- Diffrazione di raggi X (XRD)
- Tecniche superficiali
- EDX o microsonda
- Spettroscopie fotoelettroniche e spettroscopia Auger
- Analisi per attivazione neutronica
- Spettroscopia al plasma
- Spettroscopia SEM-EDS
E’ l’altro gruppo delle tecniche spettroscopiche: è più elementare, perché il suo principio è alla base anche delle tecniche molecolari:
la radiazione assorbita (o emessa) dal campione dipende in maniera univoca dagli elementi presenti nel campione precedentemente solubilizzato.
Si possono fare sia analisi quantitative che qualitative, basandosi su queste proprietà:
- ANALISI QUANTITATIVA: la quantità di radiazione assorbita dipende dal numero di atomi di analita presenti nella soluzione (dalla sua concentrazione); ma è molto difficile da usare.
- ANALISI QUALITATIVA: ogni tipo di atomo assorbe lunghezze d’onda diverse, facendosi individuare facilmente nello spettro mediante il riferimento agli standard.
SOLUBILIZZAZIONE E ATOMIZZAZIONE DEL CAMPIONE: Prima di venire utilizzato, un campione deve venire solubilizzato e quindi atomizzato.
COOP: STUDI DI PROVENIENZA: Le spettroscopie atomiche si prestano particolarmente bene agli studi di provenienza, ovvero lo studio delle varianti che uno stesso tipo di materiale subisce in diverse zone, dovute a varianti dei Sali, o di altre micro-sostanze che si trovano con essi in natura o come vengono lavorati (i marmi sono in natura di tipi diversi, mentre le ceramiche venivano lavorate insieme ad altri materiali nelle diverse città. La spettrometria si presta particolarmente bene a questi studi perché permette di confermare le variabili.
In genere però bisogna avere un’idea precisa degli elementi che voglio trovare perché si può fare l’analisi di un solo tipo alla volta.
-
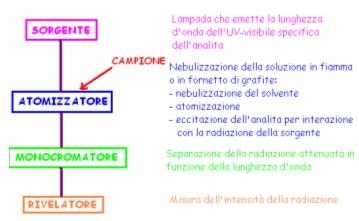
- Solubilizzazione del campione.
- Atomizzazione ad elevate temperature; chiamato anche bruciatore, in cui bruciano acetilene e aria. Nella fiamma viene immessa la soluzione che si atomizza.
- Irraggiamento con una radiazione specifica per l’analita (dell’UV-visibile).
- Interazione radiazione-atomo (transizione degli elettroni esterni allo stato eccitato). Bisogna scegliere bene la lunghezza d’onda più adatta.
- Assorbimento di radiazione.
L’analisi quantitativa è in teoria possibile misurando il rapporto tra la radiazione attenuata e la radiazione incidente in funzione della lunghezza d’onda permettendo così di costruire delle linee di taratura (per la legge di Lambert Beer) riguardo la concentrazione dell’analita, perché in teoria la radiazione assorbita (secondo la legge di Lambert Beer) dovrebbe essere direttamente proporzionale alla concentrazione del campione, con l’aiuto delle rette di taratura.
ELEMENTI INDAGABILI: si può fare praticamente con tutti gli elementi chimici che trova anche in tracce (ppm, ppb). Richiede studi precisi sulla determinazione degli elementi precisi, soprattutto in ambito mineralogico e inorganico, come metalli e pietre.
Devo più o meno sapere cosa devo indagare, perché si può analizzare un solo tipo di atomo alla volta
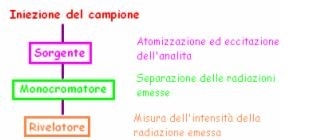
- La solubilizzazione avviene prima del processo vero e proprio, di solito con degli spray.
- Il campione poi viene messo in un plasma (= massa di gas ionizzato ad altissime temperature) dove avviene l’Atomizzazione ed eccitazione degli elementi.
- Dopodiché, l’atomo emette delle radiazioni (specifiche per ogni analita) che vengono registrate dal rivelatore, che è sensibilissimo perché deve distinguere con chiarezza gli atomi.
Si possono anche qui fare analisi quantitative perché si costruiscono delle rette di taratura, create dal rapporto tra l’intensità della radiazione emessa e la lunghezza d’onda.
L’analisi quantitativa si basa sul idea che l’estinzione della luce incidente (=log Io/I) è proporzionale al numero di atomi della sostanza assorbente per unità di volume. Tuttavia questa linearità non è perfetta e vanno costruite delle rette di taratura.
I risultati trovati vengono messi su enormi tabelle con le concentrazioni dei singoli elementi o almeno i principali (almeno 20-30) che poi vanno elaborati.
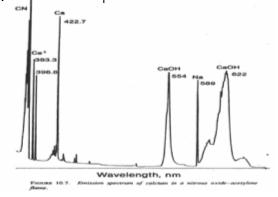
Questo è un esempio dell’assorbimento del calcio, in tutte le sue forme; possiamo notare che i picchi (sharp) si situano in lunghezze d’onda molto specifiche (indicati a volte con un numero addirittura!).
La scelta tra assorbimento o emissione atomica dipende da:
- Tipo di analita.
- Concentrazione dell’analita.
- Matrice.
Peculiarità: è possibile allestire un’apparecchiatura portatile per analisi in situ.
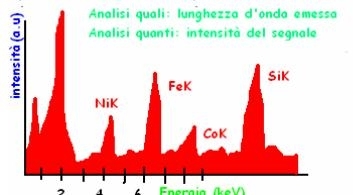
Campione: frammento oppure polvere.
Elementi identificabili: solo con elementi con numero Z superiore a 5.
Applicazioni:
- Metalli.
- Pigmenti.
- Ceramiche.
- Materiali lapidei.
- Vetri e mosaici.
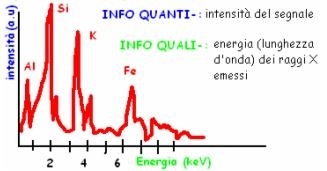
Analisi di esempio di una particella di blu di smalto del vetro. Questo schema permette di rilevare la presenza di alcuni elementi, in questo caso: Si, K, Ca, Co, As, Fe, Ni e Bi.
Tecnica analitica NON DISTRUTTIVA più diffusa.
Il fenomeno della
FLUORESCENZA SI MANIFESTA QUANDO SORGENTE ECCITATRICE E’ COSTITUITA DA RAGGI X.Per effettuare le analisi occorre:
* sorgente eccitatrice
* mezzo dispersivo
*
mezzo ricettivoLa sorgente eccitatrice è costituita da fascio di raggi x che incontra il campione da analizzare e dà luogo a fascio di raggi x policromatico che è caratteristico della natura dei costituenti del campione e che verrà riflesso in tutte le direzioni.
Fra tutte radiazioni che costituiscono il fascio incidente sul cristallo, sarà diffratto solo quella che ha lunghezza d’onda λ tale da soddisfare la relazione di Bragg
: nλ=2dsenθ;n è l’ordine di diffrazione,
d è la distanza in Angstrom fra due piani reticolari del cristallo.
La radiazione diffratta emerge sotto un angolo 2θ rispetto alla direzione del fascio incidente.
Il rilevatore è un contatore Geiger o contatore a scintillazione.
Emissione raggi x di fluorescenza: ha sensibilità che dipende dalla presenza di altri elementi cioè da composizione della matrice.
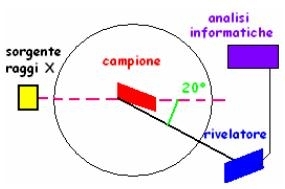
La tecnica si basa sulla diffrazione di un fascio di raggi X focalizzato sul campione.
La lunghezza d’ordine della radiazione è dello stesso ordine di grandezza delle distanze interatomiche: questo provoca FENOMENI DI DIFFRAZIONE, che dipenderanno dal reticolo cristallino delle sostanza presenti.
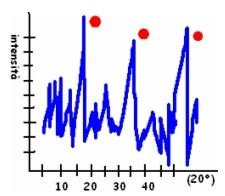
XRD permette il riconoscimento delle specie inorganiche cristalline presenti nel campione, tramite il confronto coi profili di diffrazione con standard di riferimento.
INFORMAZIONI: analisi qualitativa (profilo di diffrazione) e quantitativa (intensità dei picchi) degli analiti cristallini.
Composizione dello schema esempio: i picchi con i pallini rossi sono ossalato di calcio, ma anche sono riconoscibili gesso, calcite, silicati.
CAMPIONE: finemente macinato per evitare fenomeni d’interferenza.
APPLICAZIONI:
Analisi di:
- Malte (identificazione delle fasi di legante (calcite, dolomite) e aggregato (silicati).
- Pigmenti.
- Materiali ceramici.
- Prodotti di degrado (efflorescenze, gesso).
Funzione rilevatore nell’analisi di fluorescenza X è lo stesso che consente di caratterizzare un cristallo di un composto incognito.
Il valore della lunghezza d’onda e l'angolo di incidenza sono noti insieme ai valori di queste distanze e rappresenta l'impronta del cristallo stesso rispetto al fenomeno di diffusione di raggi X.
E' l'approccio usato per determinare in un reperto la natura dei composti cristallini (non degli elementi) presenti.
Sono tecniche basate sull’interazione di una radiazione (raggi X o elettroni) con un materiale: le interazioni provocano l’emissione di raggi X. Il fenomeno interessa SOLO la superficie del materiale indagato e pertanto è una tecnica non-distruttiva.
Analisi di tipo:
- QUALITATIVA: dipende dalla lunghezza d’onda emessa tipica di ogni elemento.
- QUANTITATIVA: dipende dall’intensità dell’onda legata alla loro concentrazione.
La radiazione incidente:
- Fascio di elettroni: spettroscopia di raggi X in dispersione di energia (EDX o microsonda).
- Raggi X: fluorescenza di raggi X (XRF).
E’ una tecnica che di solito viene accoppiata col microscopio a scansione (SEM), quindi si parla di SEM-EDX, microscopia elettronica con microsonda.
CAMPIONE: frammento o frazione lucida trasversale metallizzati (grafitatura, doratura).
PECULIARITA’:
- È possibile eseguire l’analisi elementare della stessa area (pochi μm2) visualizzata ed indagata tramite SEM
- Una volta individuata la presenza di un elemento nell’area indagata, si può cercare di mappare la sua distribuzione (analizzando tante piccolissime aree).
Manufatti indagabili:
- Materiali lapidei.
- Pitture.
- Metalli.
- Materiali tessili.
- Ceramiche.
- Vetri.
- Mosaici.
La spettroscopia fotoelettronica è di tre tipi in cui sono coinvolti fotoni come mezzo di eccitazione e sui quali viene effettuata l'analisi dell’energia degli elettroni che ne risultano:
* Spettroscopia fotoelettronica a raggi X (XPS)
* Spettroscopia elettronica Auger (AES)
*
Spettroscopia fotoelettronica in ultravioletto (UPS)XPS: impiega radiazione X come mezzo di eccitazione e registra l'energia caratteristica degli elettroni espulsi quando un atomo subisce la ionizzazione interna stimolata da fotoni o da elettroni, la vacanza risultante è occupata da un elettrone proveniente dal livello elettronico superiore.
Il processo di eccitazione può avere emissione di un fotone X o eiezione di un altro elettrone: ELETTRONE AUGER sulla misura dell’energia di tali elettroni e basata sulla spettroscopia elettronica Auger.
XPS e AES utilizzano sostanzialmente lo stesso tipo di strumentazione: hanno vario impiego in analisi di strati superficiali, patine, interfacce e di profili di concentrazione di materiali diversi e trovano crescenti applicazioni nello studio di materiali dei beni culturali.
UPS: consente di ottenere informazioni sperimentali dirette su livelli energetici degli elettroni negli orbitali molecolari. E
' il processo che attraverso l'impiego di radiazioni ultraviolette di bassa lunghezza d’onda o di raggi X di grande lunghezza d’onda permette di estrarre elettroni da molecole e prende il nome di FOTOIONIZZAZIONE.
Può essere rappresentato nella formula A+hv A++e:
l'energia del fotone hv assorbito da molecola A corrisponde a energia di ionizzazione.
Misura dell'energia di ionizzazione: permette di ottenere livelli energetici degli elettroni nella molecola che possono essere confrontati direttamente con i risultati di calcoli quanto-meccanici condotti secondo il metodo degli orbitali molecolari.
Queste tecniche permettono di indagare negli strati più superficiali dei campioni che sono quelli che interagiscono maggiormente con l'ambiente esterno.
Attivazione neutronica: metodo di analisi che si applica per la determinazione di elementi presenti in minima quantità:
si rende radioattivo un nucleo dell’elemento da dosare, quindi si rileva la radioattività emessa.All'interno dei reattori nucleari si ha la reazione di fissione dell’uranio e plutonio, che producono un grande numero di neutroni dopo essere stati rallentati da urti contro atomi del “moderatore” del reattore, urtano nuovi nuclei di uranio o plutonio, producendo nuove fissioni. Si può usare una piccola parte di questi neutroni di un reattore per attivare un certo elemento X.
Per ottenere l'attivazione è sufficiente introdurre un elemento nel moderatore in un punto che sappiamo essere attraversato da molti neutroni, alcuni di questi vengono assorbiti dai nuclei dell’elemento da dosare, essendo cioè sottratti al processo che mantiene in funzione il reattore, entro certi limiti, ciò non arresta la reazione a catena che sta alla base del funzionamento del reattore.
Quando un neutrone urta un nucleo X, possiede una certa probabilità di venire assorbito: un nucleo supposto costituito da n protoni e m neutroni e di massa (n+m) sottoposto a flusso neutroni può catturare un neutrone supplementare. La carica del nucleo non cambia.
Un neutrone possiede l'unità di massa atomica:
un nuovo nucleo possiederà massa superiore (n+m+1) e si è prodotto un isotopo artificiale di X: cioè un nuovo nucleo instabile con uno dei neutroni che si trasforma in protone emettendo un elettrone.Processo di cambio carica del nucleo: carico di una unità positiva in più.
La trasformazione non è immediata quando l'atomo X ha assorbito il neutrone, il nucleo X è instabile e si mantiene in vita per un certo tempo; gli atomi prodotti durante l'irraggiamento si conservano per un po’ ma poi sono destinati a trasformarsi nell’elemento Y il cui nucleo ha carica (
n+1) e massa (m+n+1). Conoscendo le caratteristiche del reattore e il tempo di irraggiamento possiamo sapere con sicurezza la percentuale degli atomi radioattivi prodotti.Nel campione costituito da vari elementi è probabile che oltre a X anche numerosi altri elementi vengano attivati dai bombardamenti di neutroni;
le radiazioni prodotte da questi potrebbero disturbare il conteggio di quelle; devono invece servire a rilevare la presenza e l'abbondanza di X.Per questo si procede alla separazione preliminare dei sostituenti il campione, nella misura di un elemento chimico ottenuto per attivazione. Si procede nel seguente modo: si trasforma una percentuale nota di nuclei stabili dell’elemento da cercare, in nuclei radioattivi che vanno disintegrandosi; da questi valori numerici si risale al numero di tutti gli atomi presenti nel campione analizzato.
Analisi per attivazione: si puo applicare a sostanze in forma solida, liquida o gassosa per eseguire misura precisa; basta campione di pochi milligrammi. Metodo estremamente sensibile, unico in grado rilevare alcuni elementi.
Sensibilità: dipende da flusso di particelle usate per attivazione, dalla loro energia, dalla sezione d’urto della reazione considerata, dall’abbondanza isotopica del nuclide attivato, dal fattore di saturazione ottenuto nell’irraggiamento e dal tipo di radioattivita indotta.
L'uso della spettroscopia al plasma è preferito a quello di altre tecniche analitiche: è in grado fornire la composizione chimica dei campioni; è una tecnica relativamente rapida in grado di analizzare simultaneamente più elementi con un ampio intervallo di applicabilità e rilevabilità.
Plasma: gas ionizzato costituito da ioni ed elettroni a elevata temperatura capace di produrre eccitazione negli atomi che vi si trovano immersi; è superiore a quella conseguibile con qualsiasi altro mezzo
.E' caratterizzato da notevole riproducibilità; per ottenere i segnali raccolti, sono necessari pochi milligrammi campione. Ridotto in polvere e sottoposto a trattamento di mineralizzazione, per ottenere una soluzione limpida da sottoporre ad analisi strumentale.
Eccitazione del campione: avviene all’interno della sorgente al plasma scarica ICP causata da effetto di un campo di radiofrequenza su corrente di gas indotta senza contatto tra elettroni, in una corrente di argo che sale attraverso un tubo di quarzo posto all’interno di una spirale o solenoide di rame stimolata da generatore di radiofrequenze.
Segnale di radiofrequenze: crea campo magnetico variabile
H all’interno della spirale, nella corrente di gas argo.Il campo magnetico variabile induce una corrente circolare (passata) in un conduttore che serve a sua volta a riscaldarlo.
A temperatura ambiente l’argo non è un conduttore elettrico e può essere reso tale solo per riscaldamento.
Per dare inizio alla scarica ICP, viene applicata all’argo una scintilla scarica che assorbe energia dal campo magnetico variabile e si trasforma rapidamente in un plasma di scarica stabile termicamente molto caldo e spettralmente molto intenso.
Nell'analisi spettrochimica ICP si usa spesso più di una corrente di argo: una corrente di argo viene fatta passare in vicinanza delle pareti del tubo per proteggere il quarzo dall’alta temperatura della scarica. Una seconda corrente di argo trasporta il campione verso il centro della scarica producendo un cammino effettivo verso di essa.
Anche se i campioni possono essere iniettati sia come polvere che come liquidi, oggi si usa la tecnica in cui il solvente viene fatto evaporare dalle goccioline della soluzione formatasi nella camera a spruzzo con la corrente di argo; esse fluiscono nella scarica ad alta temperatura solamente come particelle secche.
L'intensità di risposta per ciascun elemento in esame deve essere tarata per un certo numero di quantità note introdotte nella sorgente di eccitazione.
Il principio di funzionamento della
SPETTROSCOPIA IN DISPERSIONE DI ENERGIA si basa su emissione di raggi X prodotti da bombardamento di un fascio di elettroni focalizzato su un campione a cui è associato un valore di energia caratteristico di ciascun elemento.L'insieme di transizione tra livelli atomici dà luogo a insieme di raggi X distribuiti secondo uno spettro discreto di energia: permette di risalire in modo univoco all'identificazione della presenza dell’elemento stesso nel campione.
Da un confronto dell’analisi dei picchi con quella ottenuta da uno standard si può risalire alla concentrazione dell'elemento.
L'interazione elettrone-materia non si limita a una sola parte superficiale del campione, ma si estende al volume al di sotto di questa, che, in funzione sia del potenziale di accelerazione applicato sia a densità del materiale può arrivare fino alla profondità di alcuni micrometri.
Portale "Ingegneria e
Campanologia" -
Autore -
Sommario
- Mappa del Sito -
Home
Dispense tratte da: http://doc.studenti.it/download/skip/chimica-ambiente-beni-culturali_1.html (nel 2012, ora il sito non è più esistente)
Bib-TS-086 - M. Matteini, M. Moles, la Chimica nel restauro, Nardini editore, Firenze
7 - M. Matteini, M. Moles, Scienza e restauro, Nardini editore, FirenzeBib-TS-088 - L. Appolonia, S. Volpin, Le analisi di laboratorio applicate ai beni artistici policromi, casa editrice il Prato, Padova